カネカ 独自の検体処理技術を用いた新型コロナウイルスPCR検査キットを発売
株式会社カネカ IR・広報部
2020年10月8日
2020年10月8日
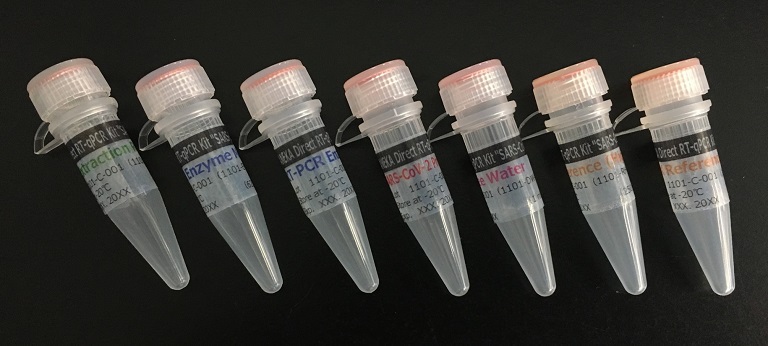
株式会社カネカ(本社:東京都港区、社長:田中 稔)は、新型コロナウイルスを1時間以内に検出可能なRT-qPCRキット(製品名: KANEKA Direct RT-qPCR Kit“SARS-CoV-2”、以下、本製品)を、10月7日より医療機関および検査施設向けに販売開始いたしました。
本製品は希望小売価格110,000円(検査100回分)で、グループ会社である株式会社カネカメディックス(本社:大阪府大阪市、社長:石坂 昌三)が販売します。
本製品は、当社が取り組んできた遺伝子検査関連製品などの技術を活かして開発した、独自の検体処理技術を採用しております。通常は必要とされる唾液や鼻咽頭ぬぐい液から採取した検体からのウイルスRNA*1精製工程が不要であり、熱処理だけで前処理工程が完了します。これにより従来法では約1時間を要していた前処理工程をおよそ5分に短縮することで、PCR検査全体の所要時間を従来の2~3時間から大幅に短縮し、1時間以内の判定が可能となりました。
本製品は、当社が取り組んできた遺伝子検査関連製品などの技術を活かして開発した、独自の検体処理技術を採用しております。通常は必要とされる唾液や鼻咽頭ぬぐい液から採取した検体からのウイルスRNA*1精製工程が不要であり、熱処理だけで前処理工程が完了します。これにより従来法では約1時間を要していた前処理工程をおよそ5分に短縮することで、PCR検査全体の所要時間を従来の2~3時間から大幅に短縮し、1時間以内の判定が可能となりました。
製品評価については、株式会社AVSS(本社:長崎県長崎市、社長:小林 信之)と共同で、国立感染症研究所の基準に則って実施しております。
本製品は、厚生労働省の「臨床検体を用いた評価結果が取得された2019-nCoV 遺伝子検査方法について*2」に掲載されており、行政検査および公的医療保険の適用対象になります。今後、医薬品医療機器等法に基づく体外診断用医薬品として承認取得を目指す計画です。
当社は新型コロナウイルスを始めとする感染症対策の研究開発を進める「インフェクション研究チーム」を立ち上げ、本製品の他、DNAワクチンの中間体製造、「アビガン」の原薬供給、ベルギーでのPCR検査試薬供給など、新型コロナウイルス問題の課題解決に向けて幅広く取り組んでいます。今後も当社の持つさまざまな技術を結集し、感染症対策に必要なソリューションを提供してまいります。
以 上
- 新型コロナウイルス特有の遺伝子のこと。ウイルスRNAをPCR検査で増幅させ、感染の有無を検出する。
- 厚生労働省および国立感染症研究所によって精度や汎用性が確認された検査方法については、検査方法を普及させる観点から、PMDA(独立行政法人 医薬品医療機器総合機構)の製造販売承認を得ることなく公的医療保険が適用されるとともに、行政検査でも使用可能となる。
<株式会社AVSSの概要>
- 本社
- 長崎県長崎市
- 代表者
- 小林 信之
- 事業内容
- 抗ウイルス剤の評価受託、開発
- 設立
- 2006年
- 備考
- 長崎大学 感染分子薬学研究室発のバイオベンチャー企業